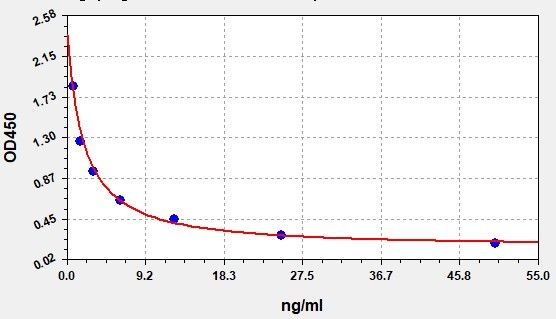
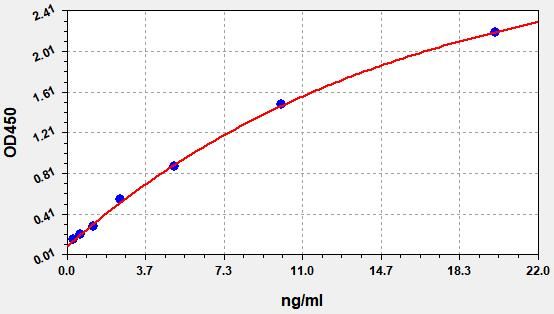
Rat TIMP-2 (Tissue Inhibitors of Metalloproteinase 2) ELISA Kit
Contáctenos para saber el precio
Por favor contáctenos para obtener información detallada sobre el precio y disponibilidad.
Name
Rat TIMP-2 (Tissue Inhibitors of Metalloproteinase 2) ELISA Kit
Category
ELISA Kits
Provider
FineTest
Reference
ER0065
Tested Applications
ELISA
Documentos del producto
Instrucciones
Data sheet
Especificaciones del producto
| Category | ELISA Kits |
| Reactivity | Rat |
| Detection Method | Colorimetric |
| Assay Data | 4 hours |
| Assay Type | Sandwich ELISA, Double Antibody |
| Test Range | 0.313-20ng/ml |
| Sensitivity | 0.188ng/ml |
| Size 1 | 96T |
| Tested Applications | ELISA |
| Sample Type | Serum, Plasma, Cell Culture Supernatant, cell or tissue lysate, Other liquid samples |
| Availability | Shipped within 10-14 working days. |
| Storage | 2-8 °C for 12 months |
| UniProt ID | P30121 |
| Alias | Metalloproteinase inhibitor 2, CSC-21K, Tissue inhibitor of metalloproteinases 2, TIMP-2, TIMP2 |
| Background | Elisa kits for TIMP2 |
| Status | RUO |
Productos relacionados

Guinea pig Metalloproteinase Inhibitor 2 (TIMP2) ELISA Kit
Guinea pig Metalloproteinase Inhibitor 2 (TIMP2) ELISA Kit is an ELISA Kit for the in vitro quantitative measurement of …
Ver producto
Pig Metalloproteinase Inhibitor 2 (TIMP2) Protein
Pig Tissue Inhibitors Of Metalloproteinase 2 (TIMP2) Protein is a recombinant Pig protein expressed in E. coli.…
Ver producto